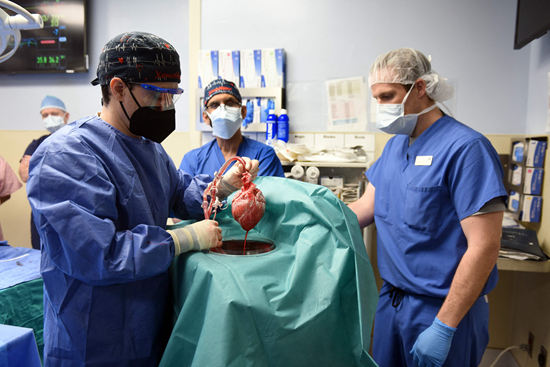
最近,美国一名57岁的晚期心脏病患者贝内特先生接受了基因编辑猪心脏移植手术。想要弄清楚为什么要移植猪的心脏,首先要明白为什么不能使用人的心脏。
根据全球捐献和移植数据库数据,2020年全球共实施129681例器官移植手术,平均每小时开展17.5例。器官捐献数量为40608例,仅能满足不到10%的全球移植需求。
心脏移植则更为特殊。与肝、肺、肾脏等器官不同,心脏移植的供体必须是已判定为脑死亡并配型成功的人。此外,在所有器官当中,心脏对器官摘除、冷藏过程中的缺血最为敏感,保存也相对不易。
这让人们逐渐把目光从人类转向了动物。
异种移植的历史超乎人们想象。早在1682年,外科医生乔布·简斯祖·范·米克伦就给一位在战斗中受伤、头骨少了一块的俄罗斯贵族安上块狗的骨头。之后的几百年,人们天马行空地进行了许多试验:青蛙的皮肤、兔子的眼睛……但最终都以失败告终。
正经的异种器官移植,还是从20世纪开始。20世纪初,法国人卡雷尔发明了血管缝合术,器官移植终于看到希望,但结局并不美好。
横亘在动物器官和人体之间的阻碍主要是免疫排斥反应。器官由供体转移到受体,受体的身体发现外来的器官,就会把它当做入侵的敌人,触发免疫反应攻击器官,病人的身体内部就成了惨烈的战场,虚弱的病人难以承受。
物种在进化的距离上越远,移植的危险也就越大。如此看来,最好的供体选择似乎应该不是猪,而是与人类亲缘更近的灵长类动物。为什么不选“大师兄”,偏要用“二师兄”呢?
从20世纪60年代开始,人们一直在尝试使用狒狒等灵长类动物的心脏、肾脏和肝脏进行移植。1983年,美国一位心脏学家为一名先天性心脏病、无法得到其他婴儿器官捐献的女婴移植了一颗狒狒的心脏。起初一切正常,在医院的新闻发布会上,她被描述为一个“美丽,健康的婴儿”。但最终由于免疫排斥反应,婴儿在21天后死亡。
由于数量稀少、器官大小差异、过近的亲缘导致的巨大伦理问题等,黑猩猩等灵长类动物不再被允许用于异种移植手术和研究。
猪的器官大小与人类相似,数量与繁殖速度更是不用多说。基因编辑技术可以通过编辑猪免疫系统的关键点位来实现“将猪心伪装成人心”,从而降低产生免疫排斥反应的风险。
此次猪心移植手术经过了10处基因编辑。3处基因被敲除避免免疫排斥反应,一处基因被敲除避免猪心组织移植后过度生长,6处负责“伪装”的人类基因插入到供体猪的基因组中,防止人类血液在猪心中凝结并降低免疫排斥的风险。
“手术至今已逾数周,可以说手术本身是很成功的。”清华大学医学院副教授吴宁说,“在术后24小时内为超急性期,患者会经历的免疫排斥反应主要是由于异种之间的巨大基因差异导致的,治疗团队对供体猪心进行了多项基因编辑,可以说基因差异问题已经大致解决。”其后是2周左右的急性期,患者也已经安然度过,现在需要等待的,就是以月计的慢性期和之后以年计的长期效果。“越急性越危险,下一个危险期大约在两至三个月左右,如果顺利度过,后续的免疫排斥反应的风险大大降低,但仍需密切监测。”
吴宁认为:“此外,还需要长期观察一些与手术本身无关的问题,比如人是直立行走的,与其他哺乳动物差别很大,猪心是否能够给患者带来长期疗效仍未可知。”
研究人员曾经向美国食品和药品管理局(FDA)申请过对猪心移植人体的临床试验,但遭到拒绝。FDA想让研究人员先将心脏移植到10只狒狒中,然后再继续移植到人体。这也是一种医疗技术研发的必经过程,先是动物实验,得到足够的数据支撑后再作用于人体。
这次破例的手术之前,患者的心脏丧失基本功能,反复心律失常,无法继续等待传统的心脏移植或进行人工心脏泵手术。猪的心脏是“目前唯一可行的选择”。FDA也因此批准了贝内特手术的紧急授权,但不意味着这项技术从此就可以走向千家万户。
“不管是多活一天,一周,一个月或是一年,我不知道。”贝内特的主治医生格里菲斯在接受《每日邮报》采访时说。
“尽管如此,哪怕是半年时间,也值得医学和医生为之努力。”吴宁说。
实习生 邱雨诺


 上一版
上一版






 缩小
缩小 全文复制
全文复制 上一篇
上一篇


