14周大的时候,英国女婴蕾拉·理查德被诊断出罹患白血病。在伦敦的医院里,医生告诉她父母:这是我们见过的最严重的急性淋巴细胞白血病。
通常对这么大的婴儿来说,这种病的治愈率在25%左右,但蕾拉看起来不属于这幸运的四分之一:她接受了化疗,却清除不尽体内的癌细胞;她的骨髓移植配型成功,可手术没多久,白血病还是复发了。
2015年6月,医生给出了最后的医嘱:姑息治疗,让孩子尽可能在平静中离开人世。
然而蕾拉的父母选择了另一条近乎疯狂的路——尝试一种全新的、以往从未在人类身上实践过的治疗方案。
这种“革命性的基因治疗方案”需要医生拾起“分子剪刀”,按照不同需要精确编辑基因,在蕾拉体内打一场环环相扣的“癌细胞阻击战”。
他们需要修改基因,释放出一批能够揪住癌变细胞狂揍的“主力军”,再引导它们绕过蕾拉体内的防御系统,躲过外界病菌和化疗药的“误伤”,最终顺利攻下癌细胞的老巢……
当治疗开始的时候,没有人知道前景是什么。此前,这种方法只在小白鼠身上试验过。
经过十几个星期的等待之后,“奇迹”发生了。
癌细胞能躲过化学药物,却可能躲不过被科学家改造过的免疫细胞
至少现在看来,蕾拉已经长成了一个健壮的婴儿。在几个月的治疗结束后,她拥有健康的骨髓细胞,各项身体指数也都保持正常。尽管说她“痊愈”还为时尚早,但目前的结果已经令医学界瞩目。
“她的白血病是那么有侵袭性,这简直是一个奇迹。”蕾拉的主治医生说。
看这女孩现在胖乎乎的样子,很难想象,最初,当她父母向医生求助时,伦敦大学学院儿童健康研究所细胞与基因治疗学教授,同时也是一家儿童医院免疫学顾问的瓦萨姆·卡西姆医生想到的是一种“在小白鼠身上很管用”的治疗方案。
他的想法很简单:反正孩子的病情已经别无选择,“为什么不使用新的UCART19细胞呢?”
蕾拉的父母也抱着同样的决心。“我不能眼睁睁看着女儿就那么走了。”她的父亲后来回忆说,“我宁愿她试过最新的手段,让我来赌一把好了。”
于是,伦敦的医学专家将尝试新的治疗方式,用“基因编辑”技术,为蕾拉度身定制一批“抗癌大军”,并直捣她的癌细胞巢穴。
比起传统医疗手段,这种新方式更为“聪明”。比如面对化学药物时,蕾拉体内总有一些癌细胞能机敏地找地方躲起来,并发展出耐药性。但它们却可能躲不过被科学家改造过的免疫细胞。
人类的每个细胞内都有一套基因组,其中包含着超过2万个基因。如今,科学家已经能够使用各种不同的方式,去修改细胞内的基因,“几乎就像改错别字一样简单”。
想想那场景:一个能修饰DNA序列的酶,或是一串自然的序列,经过科学家改造后,“全副武装”地被送进细胞里,找到目标位置,把那里的基因切开,按需要修修补补或是直接破坏。掌握了这种技术,人类可以关闭控制西红柿成熟速度的基因,把蔬菜的成熟期变长;或是删除某些小麦的基因,把庄稼改得“百病不侵”。
“基因编辑相对来说是本质上的治疗手段。”在一封邮件中,胚胎学家、中山大学副教授黄军就向中国青年报记者解释,“(此前治疗癌症最先进的)靶向治疗是针对基因变异特异设计治疗药物(治标),基因编辑是把基因修改正确(治本)。”
今年4月,黄军就副教授与他的同事利用临床废弃、不能正常发育的三原核胚胎尝试着使用了一回最新基因编辑技术。这也是人类胚胎基因首次被成功修改。
然而结果显示出的,是基因编辑技术尚存风险的一面。按照《科学》杂志当时的报道,在实验中存活的54个胚胎中,只有4个胚胎的基因修改成功。
两个月后,当身在伦敦的蕾拉开始尝试最新疗法时,没有人知道她会面对怎样的未来。
“现在你看她又笑又闹的。”蕾拉的父亲后来对媒体说,“在治疗开始前,这孩子已经非常虚弱,看起来特别吓人。”
这名虚弱的女婴所接受的基因编辑技术,是第一次在人类身上使用。
治疗方案只在白鼠身上试过,但它让蕾拉体内的癌细胞消失了
蕾拉的父亲还记得,当听说治疗方案只在白鼠身上试过时,他感到了恐惧。
但他并未因此迟疑,因为“我们总得做点什么”。
除了基因编辑,还有另一种“听起来很疯狂”的技术将被用在蕾拉身上。
CART技术,全称是“嵌合抗原受体T细胞”,也是一种还在试验期的治疗方式。被称为“T细胞”的免疫细胞被植入能识别白血病癌细胞的受体之后,就会成为既“认路”又能精准开炮的抗癌“主力军”。科学家给这种免疫细胞添加的“嵌合抗原受体”,在杀死癌细胞的基础上,还能分裂出一支“抗癌大军”。
自2011年以来,这种治疗方法已经在好几个对化疗没反应的白血病患者身上使用过。从表面上看,它不过是从病人身体里抽了点血,提取了一些细胞,然后把它们重新输回病人体内而已。
当这种技术第一次把一个6岁小女孩体内的癌细胞消灭干净时,她的主治医生惊呆了:“我已经做了20年的肿瘤学家了,可我从来没见过这样的事情。”
但幼小的蕾拉还要面临更多难关。
首先,经过化疗,她体内已经没有足够的免疫细胞,医院不得不采用了健康人捐献的T细胞,而由于配型成功比例非常低,被输入蕾拉体内的细胞与她甚至没有配型成功!
这下就轮到基因编辑技术大显身手了。科学家使用“分子剪刀”剪切掉捐赠者细胞上的相关基因,让蕾拉体内细胞对陌生的闯入者“视若无睹”。这意味着,直奔癌细胞而去的“主力军”齐刷刷穿上了“蕾拉队”制服,在她体内畅通无阻。
万事俱备后,仅有1毫升的UCART19细胞被注入女孩儿体内。通过静脉置管,花了大约10分钟,被科学家武装起来的抗癌部队杀进了小蕾拉的体内。
为了能让化疗药物与CART疗法互不冲突,这批被输入女孩儿体内的T细胞上还留了一道“暗门”:由于某种化疗药在消灭癌细胞的同时也会与T细胞“打架”,科学家还修改了细胞中对药物敏感的基因,让这些细胞在化疗药面前也“隐身”了。
医护人员和蕾拉的父母提心吊胆地等待了两三周时间。蕾拉独自住在与外界隔离的无菌病房内,而被改造过的T细胞,如果不出意外的话,则在蕾拉体内四处追击。基因编辑虽然不困难,但也有可能会错误切除基因,导致普通细胞变成癌细胞。
几个星期后,数据开始有变化。女孩儿体内的白血病细胞消失了。接下来的两个月,它们都没有重新出现。
基因组编辑技术避免了免疫排斥,使这种治疗方式具备了快速推广的可能
在内行人看来,英国的医学家为蕾拉选用的这套治疗方案原理非常简单。
“具体来说,CART疗法属于靶向治疗,用来杀死癌细胞。基因编辑技术用来关闭靶向治疗的T细胞的两个基因,关闭第一个是避免免疫排斥,关闭另一个是保证治疗用的外源T细胞不会伤及无辜。”北京大学生命科学学院研究员魏文胜总结道。
但学界关注的问题是:接下来呢?
“即便此刻她已经健康,还是不知道未来会怎样。她需要每个月做一次骨髓检查,很可能要终生服药。”女孩的父亲告诉媒体。
虽然直到目前蕾拉的各项指标看起来都不错,但是,要等到一年多之后,医生才敢下结论:究竟那1毫升经过人类种种设计的细胞,是根除了小女孩体内的白血病,还是暂时止住了癌细胞的脚步。
事实上,蕾拉与这些“抗癌主力军”只共度了两个多月的时光。T细胞杀灭了癌细胞,支撑着她等到新一次骨髓移植手术。捐赠者的造血细胞重建了小姑娘“被治疗消灭的整个血液和免疫系统”。
手术后,她终于可以离开病房,与父母、姐姐一块儿回家。曾经护佑她度过生命最低潮的那一管T细胞,已经被新捐献的免疫细胞杀死。
“这只是一个非常特殊的例子。”黄军就副教授告诉中国青年报记者。最初设计了治疗方案的卡西姆教授则表示:“在宣布这个诊疗方法适用于所有儿童之前,我们必须保持谨慎。”
但它的意义也是显而易见的。
“这是史上第一次用这种方式重新编辑人类的细胞,并且送回一个病人的体内。对我们来说,这是巨大的进步。”卡西姆教授说。
尤其是,帮蕾拉将白血病细胞消灭殆尽的,并不是与她配型成功的T细胞。
“基因组编辑技术的运用,绕开了从病人取细胞操作的限制。”魏文胜教授对中国青年报记者解释,这一点,使得这种治疗方式具备了快速推广的可能,
一位健康捐献者的T细胞,经过科研人员的改造后,可以输入上百位病人体内。
由卡西姆医生主持,纽约一家生物科技公司赞助,2016年,这种治疗方案将正式进行临床试验。
但对于理查德一家而言,生活已经彻底被这项未经试验的治疗方案改变。这对年轻的夫妇——一位司机,另一个是牙科诊所的接待员——用一种难以想象的方式留住了他们的孩子。
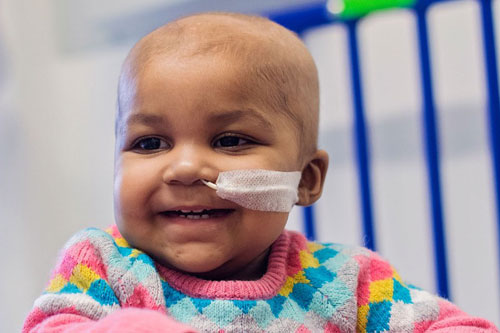
如今,除了通向鼻子的一根白色塑料管,健壮、黝黑的小蕾拉看起来与普通孩子已经没有什么不同,她玩儿着积木,“咯咯”咧开嘴大笑,样子再皮实不过。
不论经历过怎样的遭遇,至少现在,她的母亲只想感谢命运:“我想我们是非常幸运的——在正确的地方和恰当的时间,能够得到一小瓶这样的细胞。”
本报记者 黄昉苨


 上一版
上一版







 缩小
缩小 全文复制
全文复制



